一家專注于破解傳統上被認為"不可成藥"靶點的生物技術新銳公司宣布完成了1億美元的B輪融資,引發行業廣泛關注。值得矚目的是,該公司的聯合創始人之一,正是國際知名的結構生物學家、美國科學院院士吳皓教授。這不僅標志著資本對前沿靶點藥物研發的高度信心,也預示著以網絡技術與深度生物學交叉驅動的新藥開發模式,正成為攻克重大疾病難題的關鍵路徑。
一、 直擊行業痛點:"不可成藥"靶點的巨大潛力與挑戰
在傳統藥物研發中,有大量與疾病密切相關的蛋白質靶點,因其表面缺乏適合小分子藥物結合的"口袋",或與人體內必需蛋白結構功能相似等原因,難以被常規藥物(小分子或抗體)有效、安全地干預,因而被冠以"不可成藥"(undruggable)的標簽。這些靶點往往在癌癥、神經退行性疾病、自身免疫病等重大疾病的發生發展中扮演核心角色。破解這些靶點,意味著打開了通往全新療法的大門,有望為無數無藥可治的患者帶來希望。
二、 吳皓教授的科學引領:從結構解析到理性藥物設計
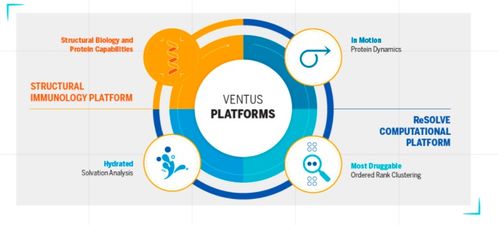
吳皓教授在細胞信號轉導、天然免疫受體以及細胞焦亡等領域的結構生物學研究享譽世界,其團隊多次在《自然》、《科學》等頂級期刊上發表重大成果,闡明了多個關鍵蛋白質復合物的精細三維結構。此次她深度參與公司創立,正是將其在復雜生物大分子結構與功能方面的深厚造詣,直接應用于藥物發現的最前沿。通過高分辨率的結構解析(如冷凍電鏡技術),團隊能夠直觀地"看見"此前難以捉摸的靶點三維形態,精準定位潛在的、可被干預的位點,從而為設計新型藥物分子(如PROTAC、分子膠、別構抑制劑等)提供至關重要的藍圖。這種基于結構的理性藥物設計,是攻克"不可成藥"靶點的核心策略之一。
三、 技術引擎:網絡技術開發賦能智能化藥物研發
本次融資消息中提及的"網絡技術開發",并非指通常意義上的互聯網技術,而是指整合并運用計算生物學、人工智能(AI)、生物信息學和大數據分析等構成的強大技術網絡。這家新銳公司的核心競爭力,很可能在于構建了一個深度整合的數字化研發平臺:
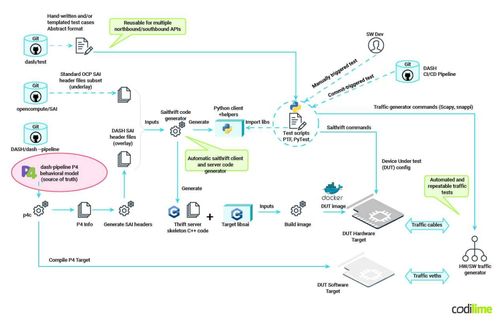
- 計算模擬與AI預測:利用超級計算機和AI算法,大規模模擬靶點與潛在藥物的相互作用,快速虛擬篩選和優化先導化合物,極大提升發現活性分子的速度和精度。
- 多組學數據整合:通過基因組學、蛋白質組學、代謝組學等多維度數據,系統描繪疾病通路網絡,識別最關鍵的靶點節點和生物標志物。
- 平臺化發現流程:將結構生物學、計算科學、化學合成與高通量實驗驗證形成閉環,打造一個可重復、可拓展的藥物發現引擎,旨在系統性地攻克一系列"不可成藥"靶點,而非單一項目。
四、 1億美元融資:信心與期望的注腳
高達1億美元的B輪融資,在當前的資本市場環境下尤為亮眼。這筆資金將主要用于:
- 推進公司核心管線中針對關鍵"不可成藥"靶點的候選藥物進入臨床前研究及臨床試驗階段。
- 進一步擴充和升級其專有的技術平臺,包括加強AI/ML能力、擴大化合物庫、提升結構解析通量等。
- 吸引全球頂尖的科研、技術及管理人才,組建跨學科的頂尖團隊。
這筆融資背后,是投資機構對于公司獨特的技術路徑、頂尖的科學創始人背景以及"不可成藥"靶點領域巨大市場潛力的高度認可。
五、 展望未來:重塑藥物研發格局
吳皓教授參與創立的這家新銳公司,代表了新一代生物技術企業的鮮明特征:頂尖基礎科研的深度轉化、前沿交叉技術的深度融合、以及挑戰終極難題的清晰愿景。其成功不僅可能催生突破性的重磅藥物,更可能驗證一種全新的研發范式。通過將最深奧的生物學洞察與最前沿的計算技術相結合,人類正在逐步瓦解"不可成藥"的魔咒。這條道路雖充滿挑戰,但正如本次里程碑式的融資所預示的,它正吸引著最聰明的頭腦和最富遠見的資本,共同邁向藥物創新的"無人區",為全球患者帶來前所未有的治療選擇。